ページ内のコンテンツを見る
臨床研究を科学性・倫理性を確保した上で実施するためには、各種の法律・規制に従う必要があります。また、臨床研究を行う前には、計画が科学的・倫理的に正しく、適正に実施可能かどうか、第三者的な審査委員会による判定を受けなくてはなりません。
ここでは、臨床研究を正しく理解し、着実に進める上で役立つ、基礎的な知識や制度について解説します。
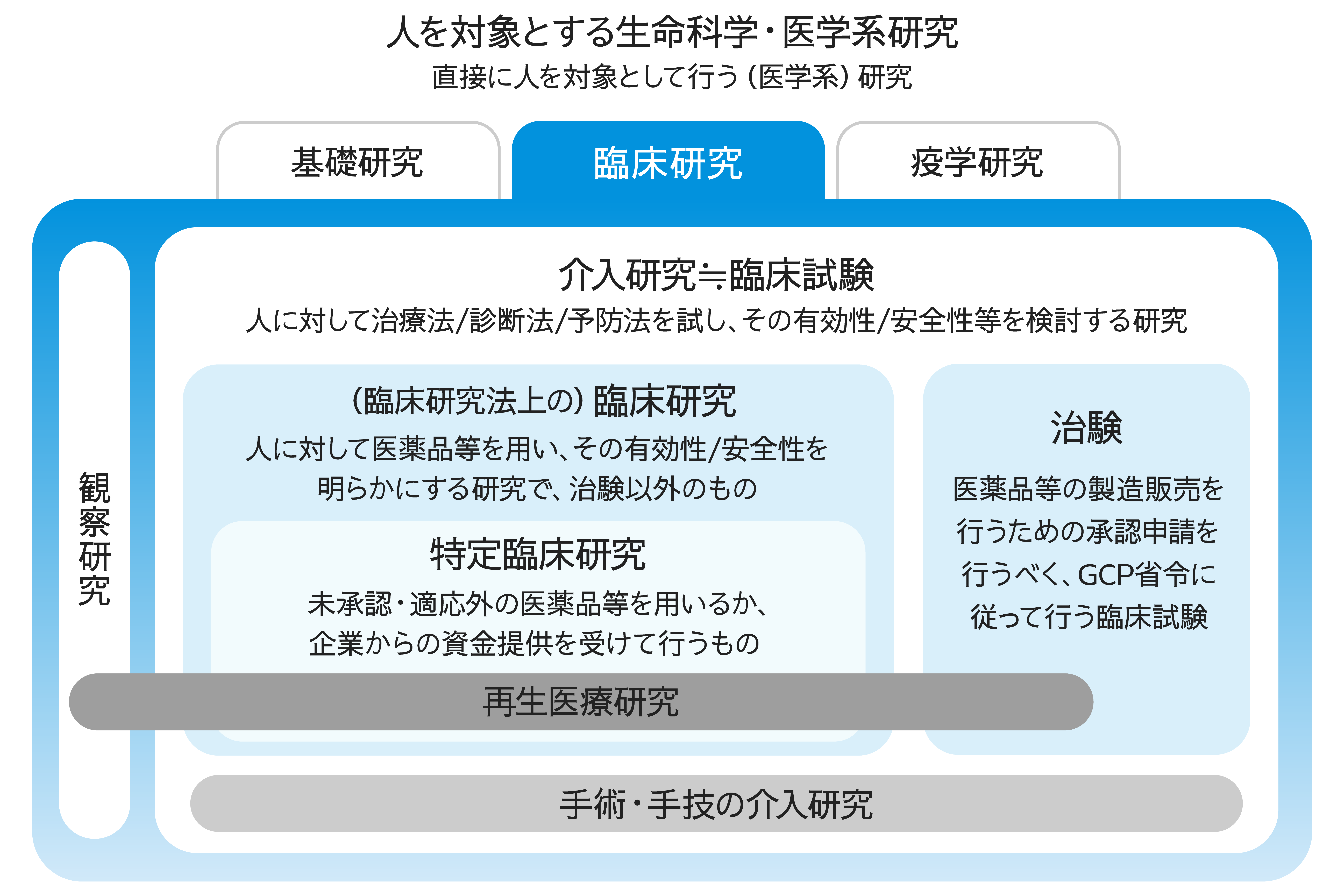
傷病の予防・診断・治療の進歩、傷病の病態の理解を目的として行う研究を「医学系研究」と呼び、その中で主に個人を直接の研究対象として扱うものを「臨床研究Clinical Research」と呼びます。
臨床研究はさらに、(通常保険診療として)都度最適な医療が行われる中でその結果を用いる「観察研究」と、診察・検査・投薬・経過観察の内容や程度を研究として制御してデータを得る「介入研究」または「臨床試験」に分けられます。
介入研究はさらに、医薬品、医療機器、または再生医療等製品(まとめて「医薬品等」と呼ぶ)の安全性や効果を見る研究と、手術・手技等の安全性や効果を見る研究とに大別されます。そして前者の中には、治験と臨床研究法上の臨床研究が含まれ、臨床研究法上の臨床研究の中にはさらに「特定臨床研究」が含まれます。