ページ内のコンテンツを見る
ページ内のコンテンツを見る
ご不明な点がございましたら、各担当までお問い合わせください。
GCP省令では、自ら治験を実施しようとする者は、あらかじめ、治験に係る被験者に生じた健康被害の補償のために、保険その他の必要な措置を講じておかなければならない、とされています。医師主導治験では、主施設が当該治験全体をカバーする保険に加入する必要があります。また、原則、治験審査委員会に申請するまでに加入していただくため、プロトコールが大まかに決まりましたら早めに下記問い合わせ先までご連絡ください。
治験審査委員会で審議される治験に関しては、治験審査委員会事務局にて、利益相反自己申告書をとりまとめ、利益相反マネジメント委員会へ提出します。
治験・臨床研究において以下の変更が生じた場合には、利益相反自己申告書を治験審査委員会事務局へご提出ください。
1.新規治験GCP省令では、医師主導治験の承認手続きについて、「自ら治験を実施しようとする者は、あらかじめ、文書を実施医療機関の長に提出し、治験実施の承認を得なければならない。」とされています。 手続きの流れは、以下のフロー図のとおりです。
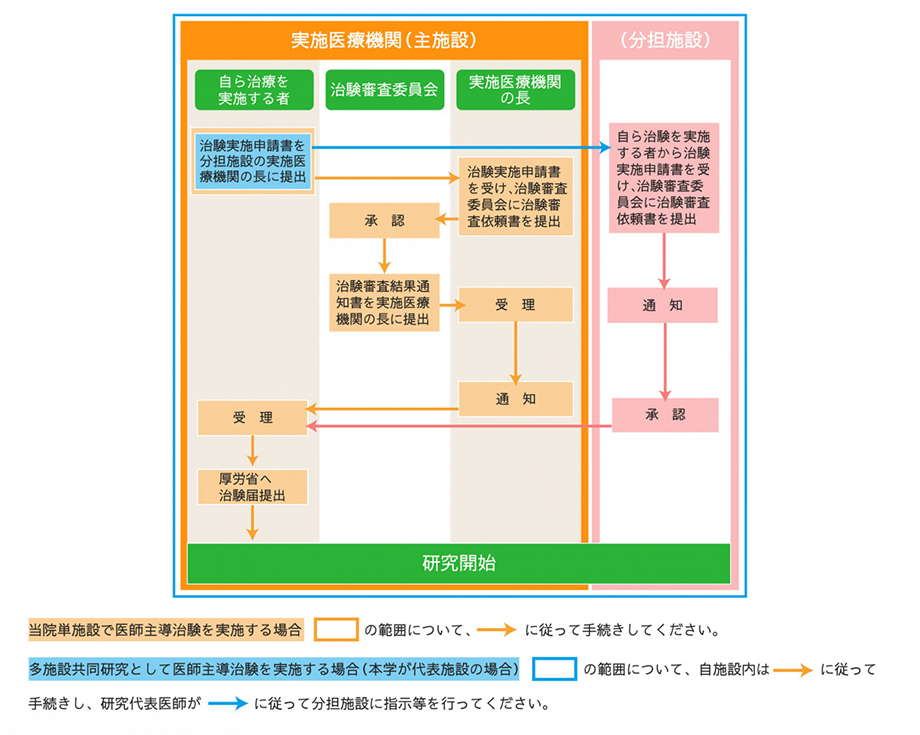 当院における治験審査委員会の承認および実施医療機関の長の通知は、事務局が窓口です。
当院における治験審査委員会の承認および実施医療機関の長の通知は、事務局が窓口です。
医師主導治験が治験実施計画書及び適用される規制要件に従って実施されていることを確認するための品質管理活動です。
研究が適切に実施されていることを治験期間を通して確認し、必要に応じて是正措置を講じるものです。
GCP省令では、医師主導治験を実施する場合は、モニタリングに関する手順書を作成し、手順書と研究計画書に定めるところにより、モニタリングを実施することを義務付けています。また、自ら治験を実施する者は、その手順書を各実施医療機関の長に提出して承認を得るとともに、IRBの承認も得る必要があります。
医師主導治験が治験実施計画書及び適用される規制要件に従って実施されていたかを評価するための品質保証活動です。
GCP省令では、医師主導治験を実施する場合は、監査に関する計画書および業務に関する手順書を作成し、治験審査委員会の意見を踏まえて、当該計画書及び手順書に従って監査を実施させなければならない、とされています。
ページ内のコンテンツを見る
ご不明な点がございましたら、各担当までお問い合わせください。
変更申請については、統一書式を用いて治験責任医師より治験事務局への提出が必要となります。
GCP省令においては、責任医師は、1年に1度医師主導治験の実施状況を治験審査委員会に報告しなければなりません。
治験責任医師は、治験審査委員会等の継続審査を受けるために、治験の現状の概要を年に1回又は当該治験審査委員会等の求めに応じてそれ以上の頻度で、実施医療機関の長に文書をもって提出すること。(GCPガイダンス第48条第1項)
実施医療機関の長は、治験期間が1年を超える場合には、1年に1回以上、当該実施医療機関において治験を継続して行うことの適否について、前条第1項の規定により意見を聴いた治験審査委員会の意見を聴かなければならない。(GCP省令第31条第1項(一部省略))
GCP省令では、自ら治験を実施する者は、被験薬について重篤な副作用を知ったときは、直ちにその旨を実施医療機関の長に通知しなければならない、とされています。
ページ内のコンテンツを見る
ご不明な点がございましたら、各担当までお問い合わせください。
GCP省令では、治験責任医師は、治験を終了したときは、実施医療機関の長にその旨及びその結果の概要を文書により報告しなければならない、とされています。
自ら治験を実施する者は、治験薬提供者が被験薬に関わる医薬品についての製造販売を受ける日、または治験の中止、もしくは終了の後、3年を経過した日のいずれか遅い日までの期間適切に記録を保管しなければならない、とされています。