ページ内のコンテンツを見る
ページ内のコンテンツを見る
ご不明な点がございましたら、各担当までお問い合わせください。
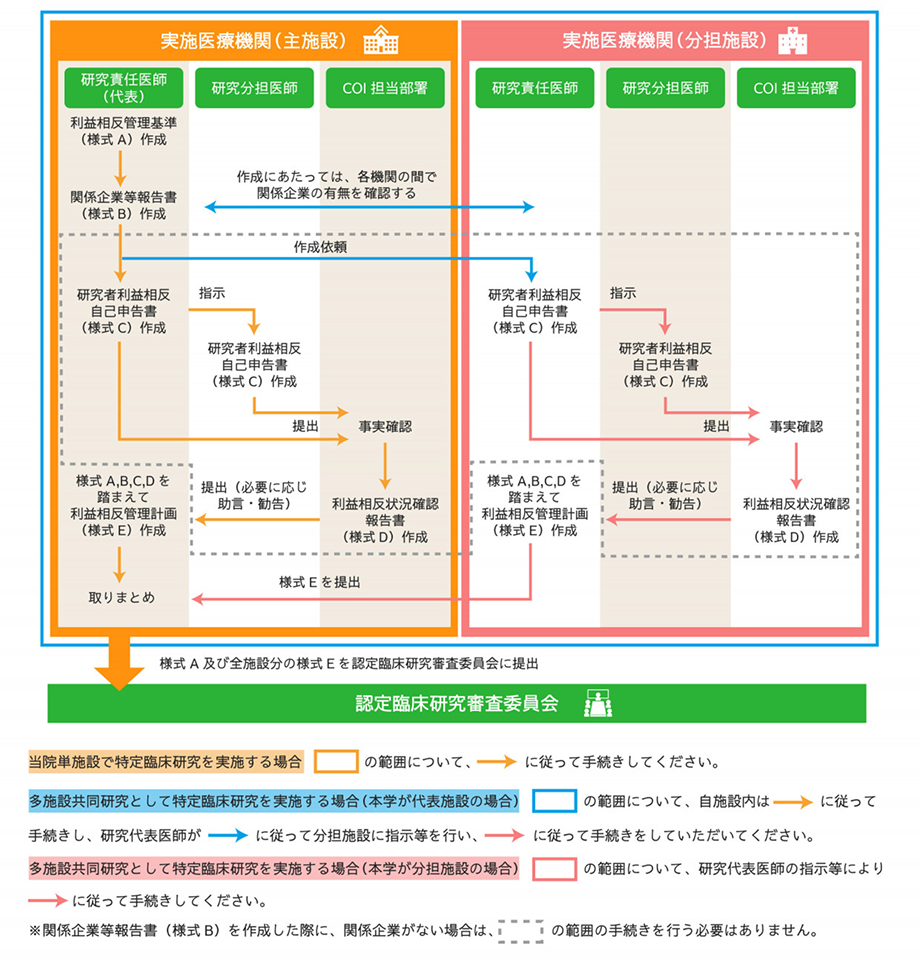
臨床研究法における利益相反に関する手続きは、従来の人を対象とする医学系研究に関する倫理指針に基づいて実施する研究と大きく異なっています。
利益相反に関する書類は認定臨床研究審査委員会での審査資料となりますので、申請時に提出が必要です。
各機関においてCOI手続きには時間を要しますので、審査申請の前に手続きを行っていただきますようお願いいたします。
臨床研究法では、「研究責任医師は、臨床研究を実施するに当たっては、あらかじめ、当該臨床研究の実施に伴い生じた健康被害の補償及び医療の提要のために、保険への加入、医療を提供する体制の確保その他の必要な措置を講じておかなければならない」(臨床研究法施行規則第20条)とされており、これについて関係通知の中で、原則として適切な保険に加入することとされています。
これを受けて、当院では、特定臨床研究を実施するにあたって、原則臨床研究保険に加入することを義務とします。
※法施行前から継続して実施している特定臨床研究で臨床研究保険に未加入のものについては、新たに保険に加入することは不要とされています。
臨床研究保険における補償の内容は大きく「医療費」「医療手当」「補償金」の3つに分けられます。
| 医療費 | 健康保険等からの給付を除いた研究対象者の自己負担額を補償する |
|---|---|
| 医療手当 | 入院を必要とするような健康被害にあっては、病院往復の交通費や入院に伴う諸費用を賄う趣旨で、一定の医療手当を支払う |
| 補償金 | 臨床研究に起因する健康被害により死亡した場合または障害が残った場合は、一定の基準により、補償金を支払う |
従来の臨床研究保険の商品では、上記のうち「補償金」についての商品しかなく、がんに関する臨床研究などは他の臨床研究と比して健康被害の発生確率が高いという理由等により、保険料が極めて高額になる、もしくは保険引受不可ということもありました。
臨床研究法において臨床研究保険への加入を原則義務化されるにあたり、補償金型の保険が適用できない場合であっても、医療費・医療手当の保険への加入により何らかの補償が可能になるよう、医療費・医療手当の保険商品が新しく導入されています。
そのため、臨床研究法における臨床研究保険への加入については、「第一の選択として補償金型の保険に、第二の選択として医療費・医療手当型の保険に加入することが望ましい」(臨床研究法の施行等に関するQ&A(その1)より)とされています。
上記4社が臨床研究保険を販売しています。各社とも臨床研究に起因して健康被害が発生した場合の賠償責任(医療行為を除く)と補償責任を保険金の支払い対象としており、免責や支払限度額などに細かな違いはありますが、補償範囲はほぼ同じです。保険各社によって保険料が大きく異なるケースがありますので、加入を検討する際は、4社の見積もりを比較することを推奨します。
保険料は研究責任医師の負担(研究費等での負担)となります。
なお、病院 基礎・臨床研究支援課研究管理係にご連絡いただければ、代理店を通して複数社の見積もりを一括入手することができます。加入をご検討の際は、以下までお早めにご連絡ください。
見積時必要書類
通常2〜3週間程度で保険会社から見積の回答が届きます。
加入時必要書類
※研究開始後、研究計画書(プロトコール)の変更があった場合は、臨床研究保険の変更手続きが必要となる場合がありますので、担当係へご連絡ください。
特に、研究実施期間の変更、症例数の変更、多施設実施機関数の変更等は、保険料の追徴・返戻が発生する可能性があります。遡及して手続きをすることはできませんのでご注意ください。
臨床研究法では、特定臨床研究の承認手続きについて、「研究責任医師は、認定臨床研究審査委員会の意見を聴いた後に、前項各号に規定する書類(実施計画や研究計画書等、認定委員会に提出した書類です)その他実施医療機関の管理者が求める書類を提出して、当該医療機関における当該特定臨床研究の実施の可否について、当該管理者の承認を受けなければならない」とされています。 手続の流れは、以下のフロー図のとおりです。
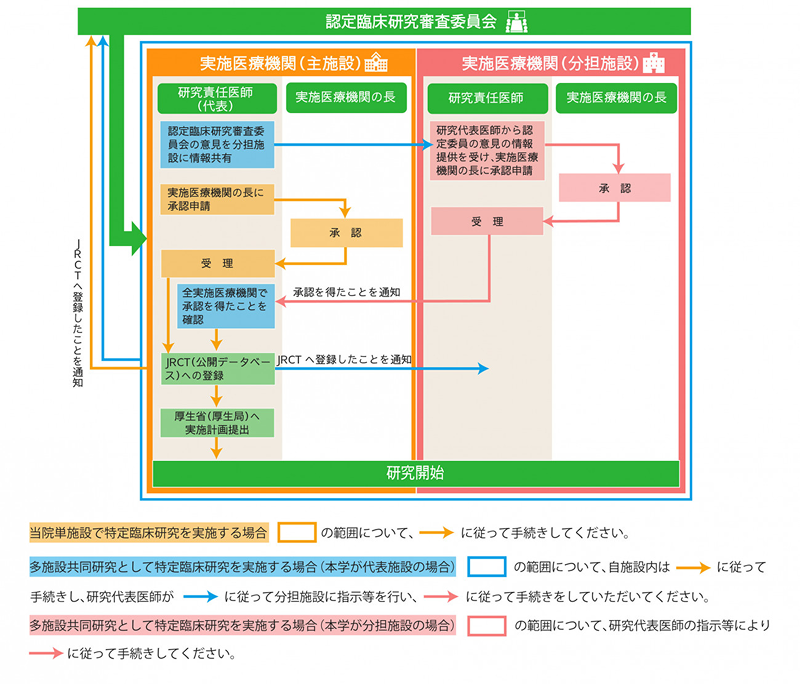
当院における実施医療機関の長の承認は、病院 基礎・臨床研究支援課研究管理係が窓口です。
以下のとおり申請をお願いいたします。
| 申請先 |
病院 基礎・臨床研究支援課研究管理係 r-kenkyu*adm.niigata-u.ac.jp(*を@に変更してください) |
|---|---|
| 必要書類 |
①認定臨床研究審査委員会に提出した審査書類の写し一式 ②認定臨床研究審査委員会の審査結果通知書 |
| 申請時期 | 認定臨床研究審査委員会の承認意見を得たのち速やかに |
※新潟大学CRBで審査した場合は、自動的に手続きされます。
ページ内のコンテンツを見る
ご不明な点がございましたら、各担当までお問い合わせください。
臨床研究法では、作成する実施計画の中に、「特定臨床研究の実施状況」という項目があり、特定臨床研究の実施状況に応じて、当該欄の変更を行う必要があります。
この変更は、変更申請手続きにより行う必要があります。従来の臨床研究においては、変更申請というと研究計画書や同意説明文書の改訂などが想定されますが、臨床研究法においては、これら進捗状況の変更についても変更申請が必要となりますので、ご注意ください。
なお、認定臨床研究審査委員会(CRB)での審査が必要です。簡便審査となる場合があります。
特定臨床研究においては、研究責任(代表)医師は、1年に1度特定臨床研究の実施状況を認定臨床研究審査委員会(CRB)に報告しなければなりません。また、同様に厚生労働大臣にも報告の義務があります。
特定臨床研究実施者は、厚生労働省令で定めるところにより、定期的に、特定臨床研究の実施状況について、当該特定臨床研究の実施計画に記載されている認定臨床研究審査委員会に報告しなければならない。(臨床研究法第17条)
特定臨床研究実施者は、厚生労働省令で定めるところにより、定期的に、特定臨床研究の実施状況について、厚生労働大臣に報告しなければならない。(同18条)

手続きの詳細については、新潟大学中央臨床研究審査委員会ホームページをご参照ください。
臨床研究法では、特定臨床研究の実施に起因するものと疑われる疾病、障害若しくは死亡又は感染症(疾病等といいます)の発生を知ったときは、病院長に報告の上、認定臨床研究審査委員会に報告をしなければならないとされています。 認定臨床研究審査委員会への報告については、疾病等の種類・程度等により報告期限が定められており、そのうち一部のものは厚生労働省に対しても報告の義務があります。
詳細および手続きについては、新潟大学中央臨床研究審査委員会ホームページをご参照ください。
臨床研究法では、臨床研究が省令または研究計画書に適合していない状態(不適合)であると知ったとき、研究責任(代表)医師は、以下の対応をしなければならないとされています。
発生した不適合の重大性に応じて、所定の様式にて報告書を作成の上、適切な報告先へ速やかに提出してください。(*を@に変更してください)
| 重大性 | 不適合 (非重大) |
重大な不適合 |
|---|---|---|
| 報告書 | 院内様式:不適合報告書 | 統一書式7:重大な不適合報告書 |
| 報告先 | 病院長:基礎・臨床研究支援課 (r-kenkyu*adm.niigata-u.ac.jp) |
病院長:基礎・臨床研究支援課 (r-kenkyu*adm.niigata-u.ac.jp) + CRB事務局 (crbcr*adm.niigata-u.ac.jp) |
以下のフローに準じて、ご報告ください。研究の実施体制及び発生施設別の例:①~④も適宜ご参照ください。
※当院以外では手続きが異なる場合があります。
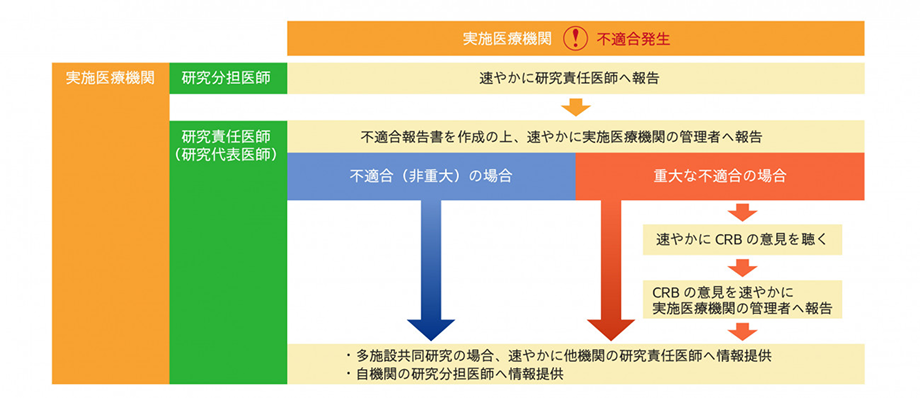
研究の実施体制及び発生施設別の例:①~④を図の形式にしたものです。あわせてご参照ください。
※当院以外では手続きが異なる場合があります。
臨床研究法においては、特定臨床研究を中止した時は、その中止の日から10日以内に、その旨を認定臨床研究審査委員会に通知するとともに、厚生労働大臣に届け出なければならない、とされています。
特定臨床研究を中止する場合は、研究対象者に適切な措置を講じてください。
また、中止届を提出した場合においても、終了の手続き(=総括報告書の作成)は必要になります。総括報告書の提出が研究終了となりますので、それまでの期間においては、研究が継続している扱いになります。引き続き、疾病等報告や定期報告、進捗状況の変更があれば変更申請が必要になりますので、ご注意ください。
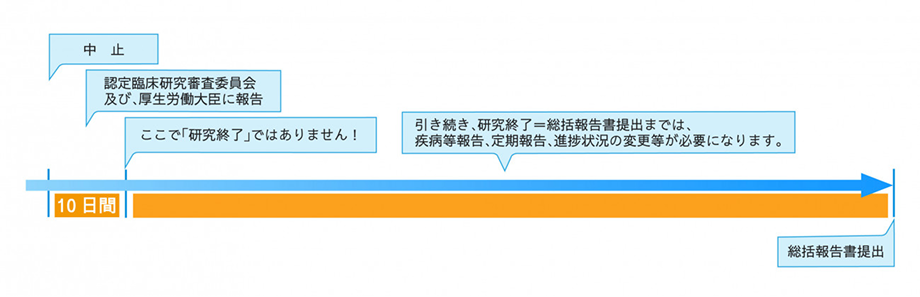
手続きの詳細については、新潟大学中央臨床研究審査委員会ホームページをご参照ください。
モニタリング、監査ともに臨床研究において内容をチェックする活動、というイメージかと思いますが、モニタリングと監査には以下のような違いがあります。
| モニタリング | 臨床研究が研究計画書及び適用される規制要件に従って実施されていることを確認するための品質管理活動。研究期間中に実施するもので、研究が適切に実施されていることを研究期間を通して確認し、必要に応じて是正措置を講じるものです。 |
|---|---|
| 監査 | 臨床研究が研究計画書及び適用される規制要件に従って実施されていたかを評価するための品質保証活動。研究期間終了後に実施するもので、試験を体系的に評価し、結果に対する信頼性確保を行うものです。 |
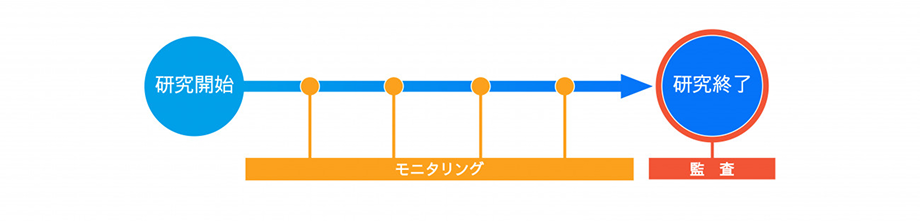
※臨床研究推進センターでは、モニタリング計画書の作成支援、チェックリストの作成等、院内でモニタリングを実施するための各種支援を行っています。お気軽にお問い合わせよりご相談ください。
臨床研究法では、特定臨床研究を実施する場合は、必要に応じて監査の手順書を作成し、当該手順書及び研究計画書に定めるところにより、監査を実施させなければならない、とされています。
「必要に応じて」とは、臨床研究の対象者数や対象者への不利益の程度、モニタリング等で見いだされた問題点、利益相反管理計画を考慮して検討することとされています。
特定臨床研究が安全かつ円滑に進むよう、被験者及び研究者を支援しています。
ページ内のコンテンツを見る
ご不明な点がございましたら、各担当までお問い合わせください。
臨床研究法では、研究の終了時期が明確にされており、総括報告書及びその概要の提出が研究の終了とされています。
従来の指針では、研究期間の終了時期が明確にされておらず、プロトコールに研究期間も統計解析含まず、症例収集・観察期間のみを記載していた方もいらっしゃると思います。
臨床研究法では、統計解析期間もすべて含めて、最終的に総括報告書の概要を厚生労働大臣に提出するまでが研究期間であり、その間も定期報告等は必要となります。
総括報告書には、少なくとも以下の項目が含まれている必要があるとされています。
総括報告書には、少なくとも以下の項目が含まれている必要があるとされています。
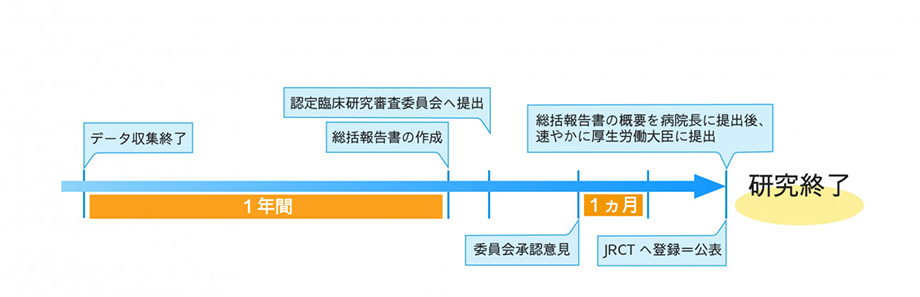
手続きの詳細については、新潟大学中央臨床研究審査委員会ホームページをご参照ください。
総括報告書以外にも終了通知書や終了届書を実施計画書とあわせて認定臨床研究審査委員会に提出する必要があります。