ページ内のコンテンツを見る
ページ内のコンテンツを見る
ご不明な点がございましたら、各担当までお問い合わせください。
人を対象とする研究等倫理審査委員会で審議される研究に関しては、本書を研究推進課・倫理審査事務局へ提出することで、利益相反マネジメント委員会で審議されます。
併せて本書のPDFを倫理審査申請システムへ掲載することにより、倫理審査委員会でも審議されます。 なお、研究責任者は研究分担者(本学所属者のみ)の利益相反自己申告書を取りまとめて、2つの委員会へ提出してください。
生命科学・医学系指針では、「侵襲(軽微な侵襲を除く。)を伴う研究であって通常の診療を超える医療行為を伴うもの」は、保険への加入その他の必要な措置を適切に講じなければならない、とされています。
本学では「侵襲を伴う研究であって介入を行う研究」を行う場合は、臨床研究保険への加入による補償を推奨しています。
臨床研究を開始(同意取得)した後では臨床研究保険に加入できなくなりますので、保険への加入を検討する場合は必ず事前に下記の担当係へご相談ください。
なお、保険料は研究責任者の負担(研究費等での負担)となります。
生命科学・医学系指針では、研究を実施しようとするときは、あらかじめ研究計画書を作成し、研究機関の長の許可を受けなければならないとされています。
本学においては倫理審査申請システムから申請を行い、倫理審査委員会(ゲノム解析等を行う研究は遺伝子倫理審査委員会。以下は代表して「倫理審査委員会」のみ記す)での審査・承認後に学長から許可されます。手続きの流れは以下のフローのとおりです。
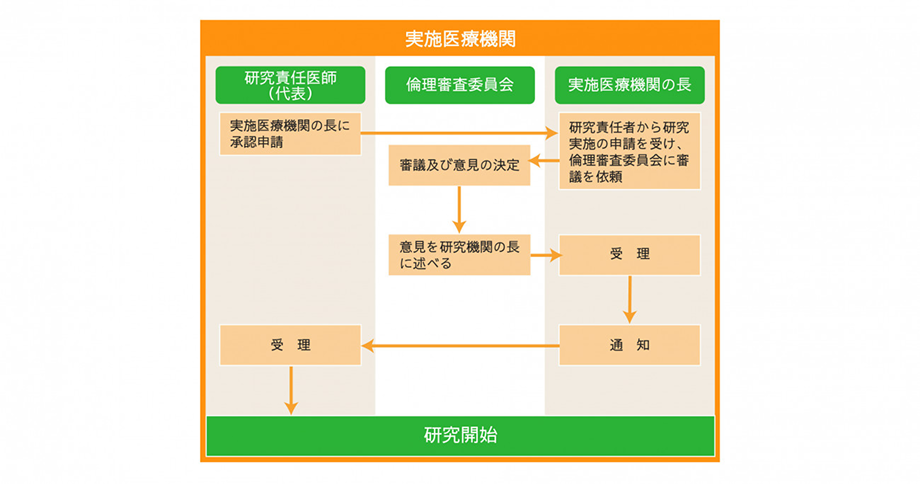
ページ内のコンテンツを見る
ご不明な点がございましたら、各担当までお問い合わせください。
生命科学・医学系指針では、研究計画書に定めるところにより、研究の進捗状況及び研究の実施に伴う有害事象の発生状況を倫理審査委員会及び研究機関の長に報告しなければなりません。
生命科学・医学系指針では、侵襲を伴う研究の実施において重篤な有害事象の発生を知ったときには倫理審査委員会に意見を聴いた上で、研究機関の長に報告しなければならない、とされています。
本学においては、倫理審査申請システムにより「有害事象報告」を学長へ報告します。
生命科学・医学系指針では、研究を中止した時は、その旨及び研究の結果概要を文書又は電磁的方法により遅滞なく倫理審査委員会及び研究機関の長に報告しなければならない、とされています。
本学においては、倫理審査申請システムにより「研究課題(終了・中止)報告書」を学長へ報告します。
生命科学・医学系指針では、侵襲(軽微な侵襲を除く。)を伴う研究であって介入を行うものを実施する場合には、モニタリング及び必要に応じて監査を実施しなければならない、とされています。
本学では、指針に規定する臨床研究で「侵襲(軽微な侵襲を除く。)を伴う研究であって介入を行うものを実施する場合」にはモニタリングを必須としています。
ページ内のコンテンツを見る
ご不明な点がございましたら、各担当までお問い合わせください。
生命科学・医学系倫理指針では、研究を終了したときは、その旨及び研究の結果概要を文書又は電磁的方法により遅滞なく倫理審査委員会及び研究機関の長に報告しなければならない、とされています。
本学における終了報告は、研究期間終了日の前に倫理審査申請システムから自動通知されるので、システムから学長へ報告を行います。